2023年11月11日,我院保红坤副研究员课题组在FKBP5通过PPAR-γ调控线粒体自噬在髓鞘再生方面取得重要进展,研究结果以“ FKBP5 activates mitophagy by ablating PPAR-γ to shape a benign remyelination environment”为题,发表在国际知名学术期刊Cell Death & Disease上。
多发性硬化症是一种常见的中枢神经系统脱髓鞘疾病,其发病因素的复杂性并伴随高致残率严重影响患者的生活质量,然而其病因和机制仍不明确,尚无有效的治疗方法。线粒体自噬通过减少活性氧(reactive oxygen species, ROS)释放抑制炎症反应有调节并促进髓鞘再生的重要功能。基因组数据显示,FKBP5是在多发性硬化症病人外周血样中检测到的高表达蛋白,但FKBP5在其中发挥怎样的作用仍不清楚。
课题组首先在野生型和Fkbp5基因敲除型小鼠中构建cuprizone (CPZ) 诱导的脱髓鞘动物模型中,发现在Fkbp5基因敲除小鼠中脱髓鞘程度明显低于野生型小鼠;随后在CPZ诱导的脱髓鞘可逆动物模型的自发恢复期分组实验中,发现再髓化进程依赖FKBP5的激活;而中枢神经系统脱髓鞘疾病总是伴随病灶处剧烈的炎症反应,该过程主要通过小胶质细胞和星形胶质细胞发生,课题组发现FKBP5的缺失严重阻碍了两种胶质细胞的富集进程;为了阐明其机制,课题组通过RNA-seq、分子对接、胼胝体脑区、BV2小胶质细胞、原代神经胶质细胞及后续分子实验系统性研究,发现了FKBP5对自噬及PINK1/Parkin介导的线粒体自噬通路的激活对髓鞘脱失和再生的进展至关重要,其中重要的调节因子PPAR-γ受到FKBP5的负调控,最终促进了中枢神经系统良性髓鞘再生环境的形成。本研究揭示了髓鞘的脱失到逐步再生的过程需要FKBP5通过抑制PPAR-γ激活线粒体自噬通路,从而促进再髓化的进程,提示FKBP5是治疗中神经系统脱髓鞘疾病的重要靶点。
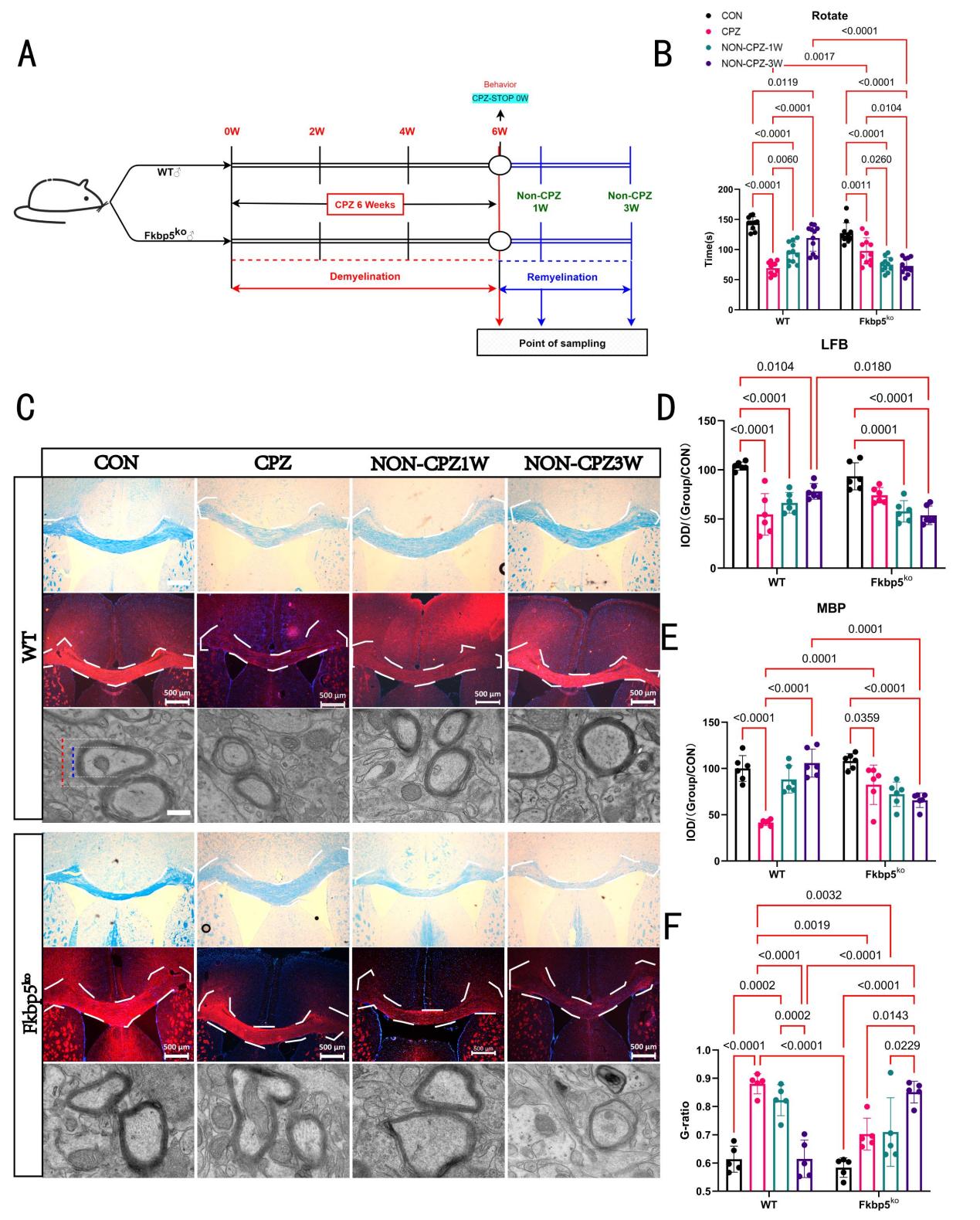
图1.(A)脱髓鞘和再髓化动物模型构建流程图、(B)动物转棒行为学统计、(C)胼胝体及周围组织区域的LFB染色、MBP荧光染色和透射电镜观察髓鞘的动态变化、(D和E)LFB、MBP的IOD统计、(F)G-ratio统计。
best365体育官网平台为该论文的第一作者单位,best365体育官网平台硕士研究生孙兴宗、钱梦寒和李宏亮副研究员为该论文的共同第一作者,best365体育官网平台保红坤副研究员、昆明学院戴利利讲师、best365体育官网平台尹敏副研究员为该论文的共同通讯作者。
该研究得到国家自然科学基金委、云南省科技厅等科学研究基金项目的共同资助。论文链接https://doi.org/10.1038/s41419-023-06260-7。